-

Génomique comparée
La génomique comparative implique l’examen et la comparaison de l’ensemble des séquences et des structures du génome de différentes espèces. Ce domaine cherche à dévoiler l'évolution des espèces, à décoder les fonctions des gènes et à élucider les mécanismes de régulation génétique en identifiant les structures et les éléments de séquences conservés ou divergents dans divers organismes. Une étude génomique comparative complète comprend des analyses telles que les familles de gènes, le développement évolutif, les événements de duplication du génome entier et l’impact des pressions sélectives.
-

Génétique évolutive
La plateforme d’analyse génétique des populations et de l’évolution est établie sur la base de l’expérience massive accumulée au sein de l’équipe R&D de BMK depuis des années. Il s'agit d'un outil convivial, spécialement destiné aux chercheurs qui ne se spécialisent pas en bioinformatique. Cette plate-forme permet une analyse de base liée à la génétique évolutive, notamment la construction d'arbres phylogénétiques, l'analyse du déséquilibre de liaison, l'évaluation de la diversité génétique, l'analyse par balayage sélectif, l'analyse de parenté, l'ACP, l'analyse de la structure de la population, etc.
-

Assemblage du génome basé sur Hi-C
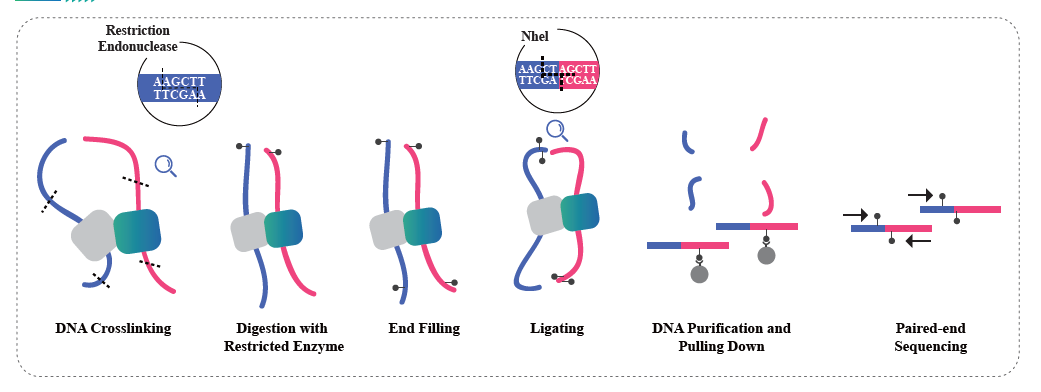
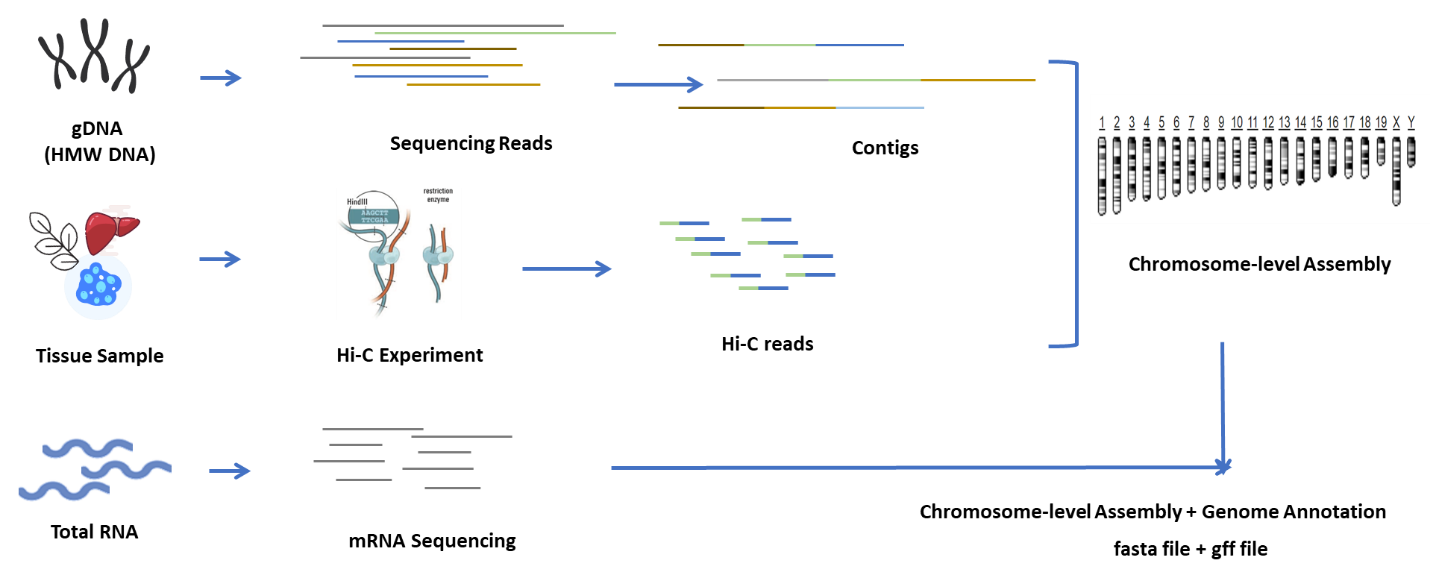
Hi-C est une méthode conçue pour capturer la configuration des chromosomes en combinant le sondage des interactions basées sur la proximité et le séquençage à haut débit. On pense que l’intensité de ces interactions est négativement corrélée à la distance physique sur les chromosomes. Par conséquent, les données Hi-C sont utilisées pour guider le regroupement, l’ordonnancement et l’orientation des séquences assemblées dans un projet de génome et pour les ancrer sur un certain nombre de chromosomes. Cette technologie permet un assemblage du génome au niveau des chromosomes en l’absence d’une carte génétique basée sur la population. Chaque génome a besoin d’un Hi-C.
-

Séquençage du génome végétal/animal de novo
De Novole séquençage fait référence à la construction du génome complet d'une espèce à l'aide de technologies de séquençage en l'absence d'un génome de référence. L’introduction et l’adoption généralisée du séquençage de troisième génération, comportant des lectures plus longues, ont considérablement amélioré l’assemblage du génome en augmentant le chevauchement entre les lectures. Cette amélioration est particulièrement pertinente lorsqu'il s'agit de génomes difficiles, tels que ceux présentant une hétérozygotie élevée, un ratio élevé de régions répétitives, des polyploïdes et des régions comportant des éléments répétitifs, des contenus GC anormaux ou une complexité élevée qui sont généralement mal assemblés à l'aide d'un séquençage à lecture courte. seul.
Notre solution unique fournit des services de séquençage intégrés et une analyse bioinformatique qui fournissent un génome assemblé de novo de haute qualité. Une étude initiale du génome avec Illumina fournit des estimations de la taille et de la complexité du génome, et ces informations sont utilisées pour guider la prochaine étape du séquençage à lecture longue avec PacBio HiFi, suivie dede novoassemblage de contigs. L'utilisation ultérieure de l'assemblage HiC permet l'ancrage des contigs au génome, obtenant ainsi un assemblage au niveau des chromosomes. Enfin, le génome est annoté par prédiction génique et par séquençage des gènes exprimés, en recourant à des transcriptomes à lectures courtes et longues.
-

Séquençage de l’exome humain entier
Le séquençage de l’exome entier humain (hWES) est largement reconnu comme une approche de séquençage rentable et puissante pour identifier les mutations pathogènes. Bien qu’ils ne constituent qu’environ 1,7 % du génome total, les exons jouent un rôle crucial en reflétant directement le profil des fonctions totales des protéines. Notamment, dans le génome humain, plus de 85 % des mutations liées à des maladies se manifestent dans les régions codantes pour les protéines. BMKGENE propose un service complet et flexible de séquençage de l'exome humain entier avec deux stratégies différentes de capture d'exons disponibles pour répondre à divers objectifs de recherche.
-

Séquençage de fragments amplifiés à locus spécifique (SLAF-Seq)
Le génotypage à haut débit, en particulier sur des populations à grande échelle, est une étape fondamentale dans les études d'association génétique et fournit une base génétique pour la découverte de gènes fonctionnels, l'analyse évolutive, etc. Au lieu d'un re-séquençage approfondi du génome entier,Séquençage du génome à représentation réduite (RRGS)est souvent utilisé dans ces études pour minimiser le coût de séquençage par échantillon tout en maintenant une efficacité raisonnable dans la découverte de marqueurs génétiques. RRGS y parvient en digérant l’ADN avec des enzymes de restriction et en se concentrant sur une plage de tailles de fragments spécifique, séquençant ainsi seulement une fraction du génome. Parmi les différentes méthodologies RRGS, le séquençage de fragments amplifiés à locus spécifiques (SLAF) est une approche personnalisable et de haute qualité. Cette méthode, développée indépendamment par BMKGene, optimise l'ensemble des enzymes de restriction pour chaque projet. Cela garantit la génération d'un nombre substantiel de balises SLAF (régions de 400 à 500 pb du génome en cours de séquençage) qui sont uniformément réparties dans le génome tout en évitant efficacement les régions répétitives, garantissant ainsi la meilleure découverte de marqueurs génétiques.
-

Bibliothèques prédéfinies Illumina
La technologie de séquençage d'Illumina, basée sur le séquençage par synthèse (SBS), est une innovation NGS adoptée à l'échelle mondiale, responsable de la génération de plus de 90 % des données de séquençage mondiales. Le principe du SBS consiste à imager des terminateurs réversibles marqués par fluorescence au fur et à mesure que chaque dNTP est ajouté, puis clivés pour permettre l'incorporation de la base suivante. Avec les quatre dNTP réversibles liés au terminateur présents dans chaque cycle de séquençage, la compétition naturelle minimise le biais d’incorporation. Cette technologie polyvalente prend en charge à la fois les bibliothèques à lecture unique et à extrémité appariée, répondant à une gamme d'applications génomiques. Les capacités et la précision à haut débit du séquençage Illumina le positionnent comme une pierre angulaire de la recherche en génomique, permettant aux scientifiques de percer les subtilités des génomes avec des détails et une efficacité inégalés.
Notre service de séquençage de bibliothèques prédéfinies permet aux clients de préparer des bibliothèques de séquençage à partir de diverses sources (ARNm, génome entier, amplicon, bibliothèques 10x, entre autres). Par la suite, ces bibliothèques peuvent être expédiées vers nos centres de séquençage pour le contrôle qualité et le séquençage sur les plateformes Illumina.