Koko genomin res.

SARS-COV-2: n genomien seuranta paljastaa NSP1-deleetiovariantin, joka moduloi tyypin I interferonivastetta
Nanopore | Illumina | Koko genomin uudelleensuuntaaminen | Metagenomiikka | RNA-seq | Pisara
Biomarkeritekniikat tarjosivat teknistä tukea näytteen sekvensoinnissa tässä tutkimuksessa.
Kohokohdat
1.SARS-COV-2-genomisekvensointi ja fylogneettinen analyysi tunnistavat 35 toistuvaa mutaatiota, mukaan lukien 31 SNP: tä ja 4 indelliä.
2.Kliinisen fenotyypin yhdistäminen 117
tärkeät mutaatiot.
∆500-532 NSP1-koodausalueella korreloi alhaisemman viruksen kanssa
3.Lataa ja seerumin IFN-p.
4.viraaliset isolaatit, joissa on ∆500-532 -mutaatio, indusoi alhaisemman IFN-I: n
vaste tartunnan saaneissa soluissa.
Kokeellinen suunnittelu

Saavutukset
1. Covid-19 epidemiologinen ja genominen valvonta
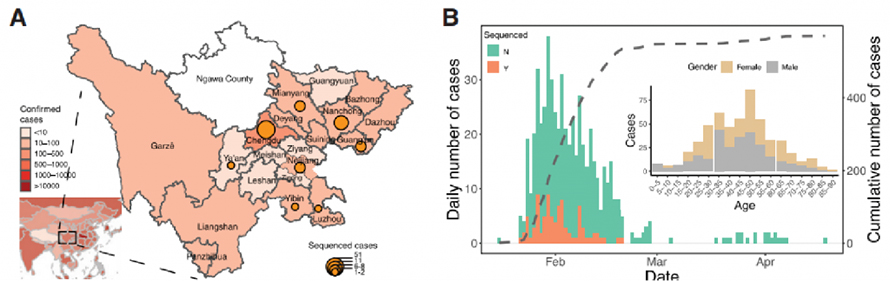
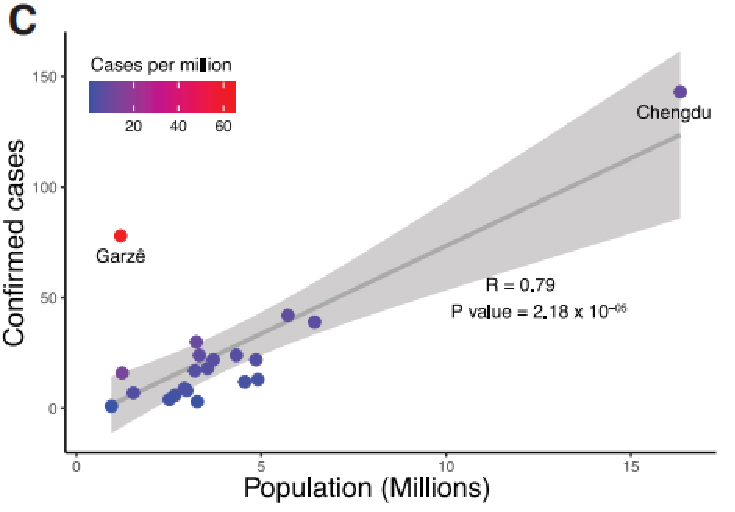
Kliiniset tiedot kerättiin Sichuanin maakunnassa, Kiinassa, koko puhkeamisen ajan 22. tammikuuta 2020-20. helmikuuta 2020. Yhteensä 538 COVID-19-tapausta vahvistettiin QPCR-testeillä Sichuanissa, joista 28,8% oli provinssista pääkaupunki. Sichuanin vahvistetut tapaukset lisääntyivät eksponentiaalisesti, huippunsa 30. tammikuuta. Tiedot tuettiin myös siitä, että sosiaalinen etäisyys voi olla avaintekijä viruksen leviämisen estämisessä.
Kuva 1. COVID-19: n epidemiologinen tutkimus Sichuanin maakunnassa, Kiinassa
2. SARS-COV-2 Genomin rakenne ja variantit tunnistaminen
Multipleksin PCR-monistuksella, jota seurasi nanopore-sekvensointi, yhteensä 310 tai osittaista täydellistä genomia 248 potilaalta tuotettiin noin. 80% 10 lukeman kattamista genomeista (keskimääräinen syvyys: 0,39 m lukee näytettä kohti).
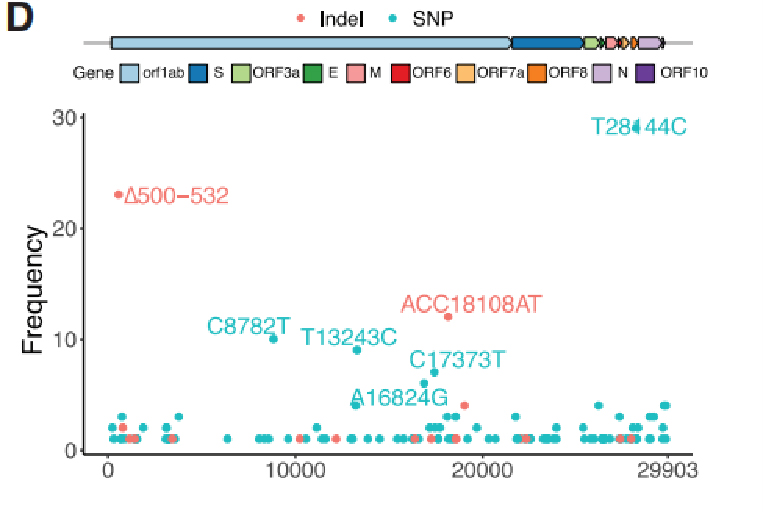
Kuva 2. Kunkin varianttien taajuus Sichuan -kohortissa
SARS-COV-2-genomeista tunnistettiin yhteensä 104 SNP: tä ja 18 indelliä, joissa 31 SNP: tä ja 4 indelliä tunnistettiin toistuviksi geneettisiksi varianteiksi. Vertaamalla niitä 169 näytteeseen Wuhanista ja 81 391 korkealaatuisilla julkaisujen genomisekvenssillä Gisaidissa, 29 muissa mantereilla esitetystä 35 variantista. Erityisesti neljän variantin, mukaan lukien ∆500-532, ACC18108AT, ∆729-737 ja T13243C, havaittiin esiintyvän vain Sichuanissa ja Wuhanissa ja puuttuivat GISAD-tiedoista, mikä osoittaa, että nämä variantit olivat todennäköisesti vääristymiä Wuhanista, jotka tapaavat The The the the the Potilaiden matkatiedot.
Evoluutioanalyysi maksimaalisen todennäköisyyden (ML) menetelmällä ja Bayesin molekyylikellohävyyksillä prosessoitiin 88 uudella viruksella Sfrom Sichuanilla ja 250 kuratoitulla genomilla muilta alueilta. Genomit, joilla oli ∆500-532 (deleetiot NSP1: n koodaavalla alueella), havaittiin jakautuneen harvoin fylogeneettiseen puuhun. Haplotyyppianalyysi NSP1 -variantteista tunnistettiin viisi niistä useista kaupungeista. Nämä tulokset viittasivat siihen, että ∆500-532 tapahtui useissa kaupungeissa ja että ne voidaan tuoda useita kertoja Wuhanista.
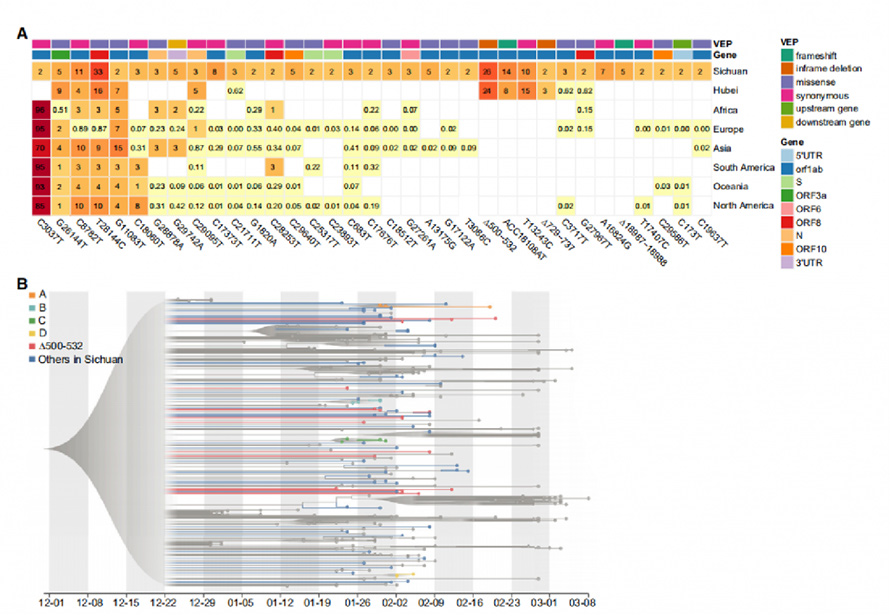
Kuvio 2. Toistuvat geneettiset variantit ja fylogeneettinen analyysi SARS-COV-2-genomeissa
3. Toistuvien geneettisten varianttien assosiaatio kliinisillä vaikutuksilla
117 Kliinisiin fenotyyppeihin liittyi COVID-19-vakavuus, jossa 19 vakavuuteen liittyvää fenotyyppiä luokiteltiin vakaviin ja ei-vakaviin piirteisiin. Näiden piirteiden ja 35 toistuvan geneettisen variantin välinen suhde viihdistettiin viihdementissä. GSEA: n kaltainen rikastumisanalyysi osoitti, että ∆500-532 korreloi negatiivisesti ESR: n, seerumin IFN-β andcd3+ CD8+ T-solujen kanssa. Lisäksi qPCR-testit osoittivat, että potilailla, jotka oli tartunnan saaneilla viruksella, jolla on ∆500-532, oli korkein CT-arvo, ts. Alhaisin viruskuorma.
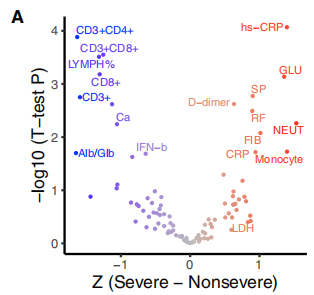
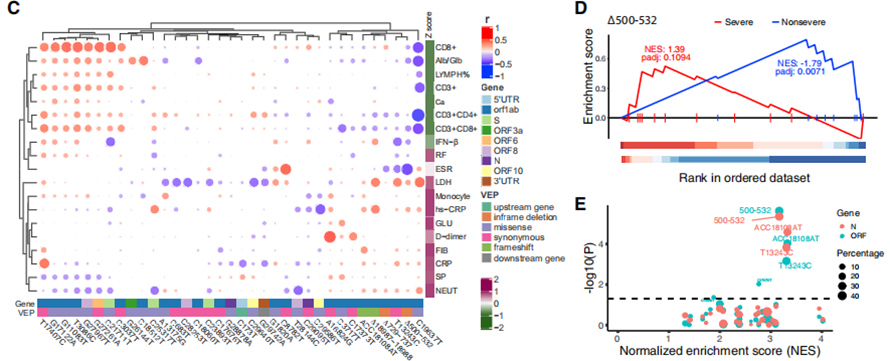
Kuvio 3. 35 toistuvan geneettisen variantin assosiaatiot kliinisillä fenotyypeillä
4. Virusmutaation validointi liittyy kliinisiin fenotyyppeihin
∆500-532: n vaikutusten ymmärtämiseksi NSP1-toiminnoissa HEK239T-solut transfektoitiin täyspitkällä, WT NSP1- ja mutanttimuodolla ekspressoivilla plasmideilla. Kunkin käsiteltyjen HEK239T -solujen transkriptoprofiilit prosessoitiin PCA -analyysiä varten, mikä osoitti, että deleetiomutantit ryhmittyivät suhteellisen lähempänä ja olivat merkittävästi erilaisia kuin WT NSP1. Geenit, jotka olivat merkittävästi ylöspäin mutanteissa, rikastuivat pääasiassa ”peptidien biosynteettisen/metabolisen prosessin”, “ribonukleoproteiinikompleksin biogeneesillä”, “proteiini, joka kohdistuu kalvoon/ER: ään" jne. Lisäksi kaksi deleetiota osoittivat erillistä ekspressiokuviota WT: stä.
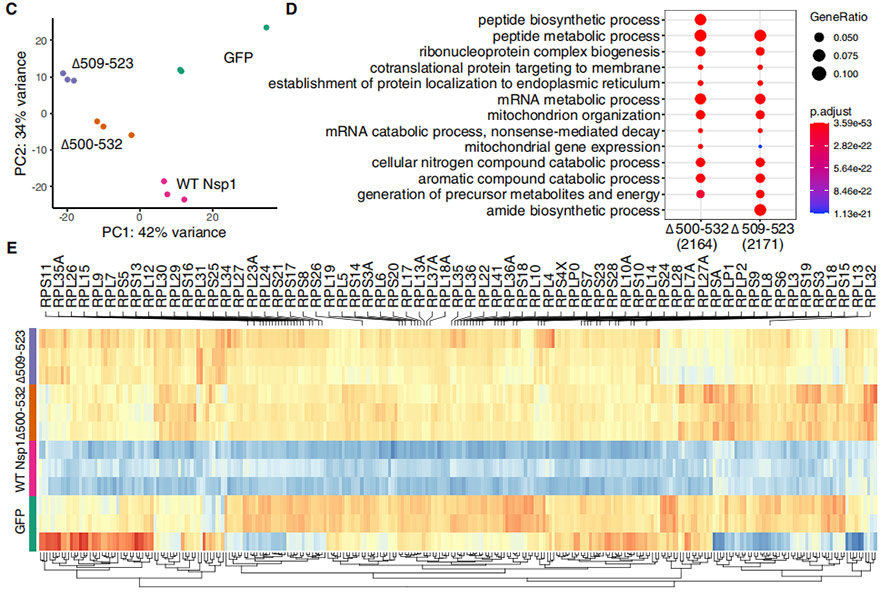
Kuvio 4. WT NSP1: n transcriptomianalyysi HEK239T -soluissa ja se deleetioilla
IFN-1-vasteen deleetioiden vaikutukset testattiin myös yliekspressoidussa tutkimuksessa. Kaikkien testattujen deleetioiden osoitettiin vähentävän IFN-1: n repsonsea transfektoiduissa HEK239T- ja A549-soluissa sekä transkriptotasolla että proteiinitasolla. Mielenkiintoista on, että deleetioiden merkittävästi alas säädetyt geenit rikastuivat ”puolustusvasteella virukselle”, “virusgenomin replikaatio”, “RNA-polymeraasi II: n transkription säätely” ja “vaste tyypin I interferonille”.
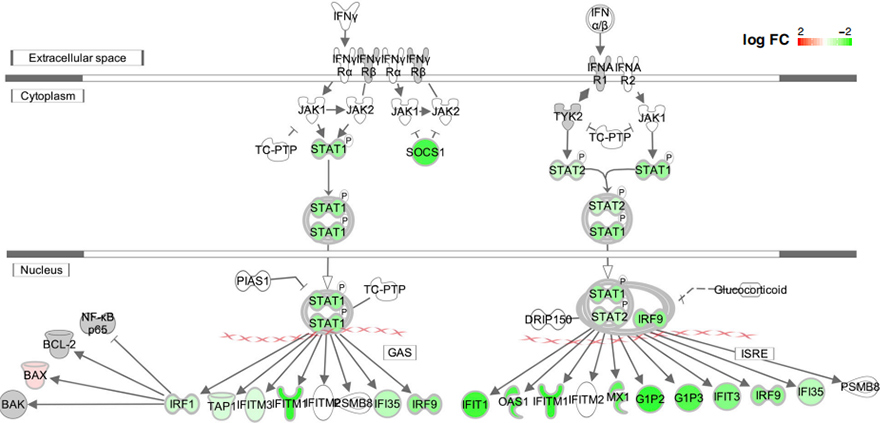
Kuvio 5. Interferonin signalointireittien säätely ∆500-532 -mutantissa
Tässä tutkimuksessa näiden deleetioiden vaikutus virukseen vahvistettiin edelleen virusinfektiotutkimuksilla. Virukset, joilla oli tiettyjä mutantteja, eristettiin kliinisistä näytteistä ja infektoitiin Calu-3-soluihin. Lehdessä voidaan lukea yksityiskohtaisia tuloksia virusinfektiotutkimuksesta.
doi:10.1016/j.chom.2021.01.015
Viite
Lin J, Tang C, Wei H, et ai. SARS-COV-2: n genominen seuranta paljastaa NSP1-deleetiovariantin, joka moduloi tyypin I interferonivastetta [J]. Cell Host & Microbe, 2021.
Uutiset ja kohokohdat Tavoitteena on jakaa viimeisimmät onnistuneet tapaukset biomarkkeritekniikoiden kanssa, vangitsemalla uusia tieteellisiä saavutuksia sekä tutkimuksen aikana sovellettuja näkyviä tekniikoita.
Viestin aika: tammikuu-06-2022


